2.云南中医学院, 昆明, 655000
 作者
作者  通讯作者
通讯作者
《分子植物育种》网络版, 2012 年, 第 10 卷, 第 27 篇 doi: 10.5376/mpb.cn.2012.10.0027
收稿日期: 2012年02月28日 接受日期: 2012年04月26日 发表日期: 2012年06月12日
引用格式(中文):
周国雁等, 2012, 适于云南小麦断穗和抗条锈病引物的SSR-PCR反应的体系优化, 分子植物育种(online) Vol.10 No.27 pp.1191-1198 (doi:10.5376/ mpb.cn.2012.10.0027)
引用格式(英文):
Zhou et al., 2012, Optimization of SSR-PCR Reaction System Adapted to Primers for Brittle Rachis and Stripe Rust Resistance in Triticum aestivum ssp yunnanense King, Fenzi Zhiwu Yuzhong (online) (Molecular Plant Breeding) Vol.10 No.27 pp.1191-1198 (doi: 10.5376/mpb.cn.2012.10.0027)
为开展云南小麦(Triticum aestivum ssp yunnanense King)断穗、抗条锈病基因的分子辅助标记鉴定,选择其新鲜幼嫩的无病斑叶为材料,研究了PCR反应体系中Mg2+、dNTP、模板DNA、引物和Taq酶的浓度对其断穗、抗条锈病SSR引物扩增结果的影响,构建起了适宜其断穗、抗条锈病基因分子标记的最佳PCR反应体系,该体系为Mg2+ 1.8 mmol/L、dNTP 0.25 mmol/L、模板DNA 30 ng、引物0.1 μmol/L、Taq DNA聚合酶1.5 U、再加ddH2O补至25 μL。此反应体系有良好的稳定性,将为开展云南小麦断穗和抗条锈病基因的SSR标记研究提供分子生物学基础。
云南小麦(Triticum aestivum ssp yunnanense King, AABBDD, 2n=6x=42),也俗称云南铁壳麦,是中国西部特有的三种小麦种质资源之一。其显著地有别于普通小麦种的特点不仅是包壳紧、不易脱粒,因而抗穗上发芽和鸟害(曾学琦等, 1989, 云南农业科技, (5): 3-6; 董玉琛等, 1981; 伍少云和奉有壁, 2001),而且还有成熟时小穗轴节片受外力影响易下节位断裂的原始特性。这种断裂方式也称楔型(陈庆富, 1999; 王志清和郑有良, 2004; Watanabe et al., 2005)断裂,是断穗发生在小穗与主穗轴连接点的上方,断裂的小穗与自己的小穗轴相连。不过,其断裂程度不及西藏半野生小麦的自然脱落(王志清和郑有良, 2004; 邵启全等, 1980; 陆平, 2000, 西藏农业科技, 22(2): 23-27)。虽然,自其在1937年被金善宝教授发现并在1959年被确定为普通小麦种云南小麦亚种(董玉琛等, 1981)以来,国内有关研究人员曾先后对其进行了分类(董玉琛等, 1981)、抗旱性鉴定(伍少云和奉有壁, 2001)、抗条锈病鉴定(李明菊, 2004; 李明菊和伍少云, 2005; 2006)、高分子量谷蛋白亚基组成及遗传多样性(王海燕等, 2005; 2007; 杨金华等, 2007)等研究,以及在研究定位西藏半野生小麦的断穗基因时,将其与西藏半野生小麦比较,得出了其控制断穗性状的基因与西藏半野生小麦的等位(陈庆富, 1999; Chen et al., 1998)或不同(陆平, 2000, 西藏农业科技, 22(2): 23-27)的结论。然而,到目前为止,其控制断穗行为的基因所在的染色体位置及其遗传机制仍没有统一的观点。另外,也未见有关其抗病基因的定位研究报道,以致因其在长期相对封闭的生产环境下种植,缺乏与外界基因的交流而是否形成有抗病新基因等也都不清楚。
少数几个核苷酸经多次串联重复的DNA序列(Tautz, 1989),即称微卫星的简单重复序列(Simple sequence repeats, SSR)的分子标记,由于具有可重复、稳定和多态性强,已成为了构建高度饱和的真核生物的基因图谱的标准和理想分子标记,是进行种质资源和品种遗传多样性分析、并确定其遗传关系的重要分子技术手段(Beckmann and Soller, 1990; Katzir et al., 1996)。但由于这种微卫星或SSR标记技术是基于PCR基础上建立起来的,因此PCR的各种反应条件,如不恰当的模板DNA、Taq聚合酶、dNTP以及Mg2+的浓度和不适宜的退火温度等都会导致获得的图谱产生弥散背景、扩增出的条带不清晰或位置改变,甚至无扩增产物等,从而最终影响对扩增产物的准确统计与分析(迪芬巴赫C.W, 和德维克斯勒G.S., 1998)。所以,在利用SSR标记进行各种研究和分析前,筛选出适合目标DNA扩增的PCR反应条件是至关重要的。鉴于目前,国内外还未见利用SSR分子标记开展云南小麦断穗或抗病基因定位或标记研究的报道,我们旨在开展此项探索研究之前,首先探讨影响PCR反应体系的各种主要成分浓度或用量对云南小麦断穗和抗条锈病SSR引物扩增结果的影响,拟筛选出各种主要成分的最佳用量或浓度量,建立适合云南小麦断穗和抗条锈病基因分子标记的最佳SSR-PCR反应体系。
1结果与分析
1.1 MgCl2浓度的筛选
由于Mg2+是聚合酶—Taq DNA的催化剂,因此它的浓度高低将直接影响dNTPs与模板DNA竞争结合的强弱、SSR引物同模板DNA结合的效率和特异扩增物的产生(林万明, 1993)。所以,合适的Mg2+浓度是获得清晰扩增条带的首选必须考虑和优化的因素之一。
采用1.4 mmol/L、1.8 mmol/L、2.2 mmol/L 和2.6 mmol/L四种不同的MgCl2浓度进行了PCR扩增实验。从图1可以看出,当Mg2+浓度在1.4 mmol/L时,由于Taq DNA聚合酶未完全被激活,只产生了很少的扩增产物,且出现了弥散现象。随着Mg2+浓度的增加催化作用也随之逐渐增强,扩增出的产物也增多,产物的浓度也增大,但当到达一定程度时,扩增产物反而减少且不清晰。所以,我们认为在1.8 mmol/L~2.6 mmol/L之间的Mg2+浓度是适合云南小麦断穗与抗条锈SSR反应的浓度,且以1.8 mmol/L的浓度产生的条带多、清晰程度高。
.png) 图1 Mg2+浓度试验结果 |
1.2 dNTP浓度的筛选
dNTP的浓度过低,不仅会影响扩增产物的合成效率,甚至会因dNTP过早消耗而使产物单链化,影响扩增效果;过高则容易引起拖尾,甚至无扩增产物。另外,无论是过高或是过低,都会使Mg2+产生拮抗作用,特别是在过低时,这种拮抗作用更为明显。因此,在建立PCR反应体系时首先应将dNTP的浓度确定在20 μmol/L~200 μmol/L之间(余艳等, 2003)的范围内。
本实验以0.1 mmol/L、0.15 mmol/L、0.2 mmol/L、0.25 mmol/L、0.3 mmol/L和0.35 mmol/L六种不同的dNTP浓度探讨了PCR的扩增(扩增效果如图2)效果。图2表明,在0.1 mmol/L的dNTP浓度时扩增出的产物很少,而在0.2 mmol/L~0.3 mmol/L时出现的产物最多,并以0.25 mmol/L时的条带多而清晰,在0.35 mmol/L时则又无扩增产物。因此,我们认为0.25 mmol/L的dNTP浓度应是云南铁壳麦SSR反应的最适浓度。
.png) 图2 dNTP浓度试验结果 |
1.3引物浓度的筛选
我们设计了0.06 μmol/L、0.1 μmol/L、0.14 μmol/L和0.18 μmol/L四种不同的引物浓度来检验PCR的扩增效果(扩增结果如图3)。从扩增出的条带多少和清晰度看,引物浓度在0.06 μmol/L以下时产生的扩增物太少,甚至根本没有扩增物,在0.1 μmol/L~0.18 μmol/L之间时不但有较多的扩增物,而且以0.1 μmol/L 时的条带效果最好。因此,我们选用0.1 μmol/L的引物浓度作为云南铁壳麦SSR反应的最适浓度。
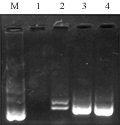 图3 引物浓度试验结果 |
1.4模板DNA浓度的筛选
实验中对10 ng、20 ng、30 ng和40 ng四种不同的模板DNA浓度进行了PCR扩增检验(扩增结果如图4)。模板DNA浓度太低,则分子碰撞的几率也越低,偶然性增大,扩增物也就不稳定;模板浓度过高则会造成条带模糊,出现弥散现象。从图4看,30 ng时扩增出的条带较其他浓度的都清晰。因此,我们选用30 ng的模板DNA作为最适浓度。
 图4 DNA浓度试验结果 |
1.5 Taq DNA聚合酶浓度的筛选
在PCR反应中,Taq酶的用量也是影响实验结果的一个重要因素。使用高浓度的Taq酶不但造成浪费,而且很容易发生高错配率、产生非特异性扩增物;过低则会导致产物的合成效率下降。在随机扩增反应中,一般应将Taq酶的浓度控制在0.5 U~5 U之间(余艳等, 2003)。
我们通过对0.5 U、1.0 U、1.5 U和2.0 U四种不同的Taq DNA聚合酶浓度的PCR扩增(扩增结果如图5)表明,Taq酶浓度在1.5 U时扩增出的产物多且较清晰,而低于1.5 U时扩增出的产物减少,但高于1.5 U时又无扩增物出现。因此,为了既不影响扩增物又避免过多的浪费,我们选用1.5 U的Taq DNA聚合酶作为云南铁壳麦SSR反应的最适浓度。
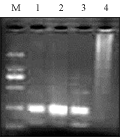 图5 Taq DNA聚合酶浓度试验结果 |
1.6建立优化的SSR反应体系
我们通过不同浓度的Mg2+、dNTP、引物、模板DNA和Taq DNA聚合酶对PCR扩增效果影响的反复实验、比较分析和筛选优化,摸索出了一套适于云南小麦断穗与抗条锈病SSR标记反应的最佳PCR反应体系,即在总体积25 μL的反应体系中,以Mg2+ 1.8 mmol/L、dNTP 0.25 mmol/L、引物0.1 μmol/L、模板DNA 30 ng和Taq DNA 1.5 U为最佳浓度或用量。其扩增程序为:94℃预变性3 min,44个循环按照94℃变性1 min、复性1 min、72℃延伸2 min进行,最后72℃延伸10 min。扩增结束后,采用2%的琼脂糖凝胶进行电泳,以确定利用该体系进行云南小麦抗条锈病和断穗基因的SSR反应是否能达到理想的扩增效果。为此,我们用与抗条锈病基因连锁的SSR引物Xgwm582和与断穗基因连锁的Xgwm161,分别对37份云南小麦和山羊草、野生一粒和乌拉尔图小麦等共47份不同的实验材料进行了扩增效果检验。扩增结果表明,在该体系下两对引物都分别在47份材料中扩增出了清晰、强弱明显的DNA条带(图6和图7),这说明利用该体系开展云南小麦抗条锈病和断穗基因的SSR标记研究是合适的和有效的。
 图6 抗病引物Xgwm582在47份小麦材料中的PCR扩增 |
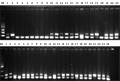 图7断穗引物Xgwm161在在47份小麦材料中的PCR扩增 |
2讨论
SSR标记虽然作为遗传多样性、物种起源、品种指纹图谱构建或个体识别和遗传辅助育种等研究的工具或技术手段已是公认的和理想的,但是如果在PCR反应体系中使用了不适宜的Taq聚合酶、Mg2+、dNTP、模板DNA和引物等成分的浓度或用量会使扩增物放大或缩小对它们的敏感性和特异性。就这些成分的单独影响而言,Mg2+浓度与Taq聚合酶活性有关,它在过低时会显著降低后者的活力,反之则又会使非特异产物增多,以致无法鉴别真正的目的产物;dNTP不仅是反应体系中的重要物质,而且它在浓度过低时会使PCR扩增效率降低,反过来,它又将同Taq聚合酶抢夺Mg2+,使Mg2+浓度降低,从而弱化Taq酶活性,并使扩增量显著减少;在反应体系中保证有足够、特异性显著且浓度适当的引物量也是利用这项工具或手段必须要考虑的因素之一,过高的引物浓度不但会增加非特异性扩增物的数量,而且还会使它自己形成二聚体;而过高的模板DNA和Taq聚合酶的浓度也会导致PCR反应中非特异性扩增物的增加,相反,则使目的产物减少(Sato et al., 2005)。除此外,这些成分之间的相互作用,如dNTP同Taq聚合酶、以及与模板DNA抢夺Mg2+等,也都对最终获得的扩增物数量和质量有较大影响。因此,在利用SSR标记这项手段开展相关的研究之前,针对要具体研究的目标首先构建起适合对象的反应体系是利用这项工具的基本条件。
我们通过对上述这些影响PCR扩增效果的成分的浓度或用量进行反复试验与优化,建立起了一套适用于云南小麦SSR分子标记研究的最佳反应体系。该体系不仅扩增出了清晰、强弱明显的谱带,而且可重复性也非常好。这将为从DNA分子水平上研究云南小麦的起源演化、系统分类、品种鉴别或抗病性基因发掘等提供分子生物学基础。
3材料和方法
3.1植物材料与试剂
本实验所用的37份云南小麦及对照小麦品种中国春来源于云南省作物种质中期保存库,陕西节节麦、中东山羊草、野生一粒小麦、乌拉尔图小麦、栽培一粒小麦、野生二粒小麦、东方小麦、波兰小麦和波斯小麦等9份材料来源于中国农业科学院作物科学研究所。这些材料的新鲜、无病斑幼嫩叶全部采自本所试验地。本实验所用的SSR引物由上海捷瑞生物工程有限公司合成,10 X buffer (含镁离子浓度18 mmol/L),dNTP和TaqDNA聚合酶则购自TaKaRa。
3.2 DNA的提取方法
我们采用改良的CTAB提取法(夏铭等, 1999; 柴建芳等, 2006)提取了所有参试材料的全基因组DNA。具体的提取过程为:称取1 g左右的参试材料的新鲜叶片,用液氮将其研磨成粉末状,装入1.5 mL的Eppendorf管中,再加入CTAB提取液(含2%的CTAB, 100 mmol/L的TrisHCl (Ph 8.0), 20 mmol/L的EDTA (pH 8.0), 1.4 mol/L的NaCl和2%的ß-巯基乙醇)充分混匀,放进65℃的水浴中保温1 h。随后,用12 000 rpm的离心机分离10 min,将上清液吸至另一离心管中,加入1/2体积的氯仿/异戊醇(24:1),轻缓颠倒混匀,用12 000 rpm的离心机再离心5 min,重新将上清液转至另一离心管,并以满足抽提两管的量为准。然后,在抽提形成的每一管中加入1/10体积的7.5 mol/L醋酸铵和等体积的冰乙醇(100%),混匀,放在-20℃的冰箱中处理30 min或室温下过夜。取出,用12 000 rpm的离心机再离心15 min,获得沉淀的DNA,用70%乙醇将该DNA清洗2次,风干沉淀。再加入TE缓冲液(含10 ng/μL RNaseA)将其溶解后,放入37℃的水浴中热处理30 min,取出,以岛津UV-120-02型紫外分光光度计测定其在260 nm和280 nm的吸光光度值,以确定其浓度和纯度,并最终将其稀释为10 ng/μg的样品,在低温下留存备用。
3.3 PCR分析方法
按表1设计的各成分浓度方案,在反应体系为25 μL的条件下,采用T-Gradiant (Biometra, 德国)PCR仪对DNA进行扩增。其扩增条件是94℃预变性3 min,44个循环按照94℃变性1 min、50℃复性1 min、72℃延伸2 min进行,最后72℃再延伸10 min,放在4℃下的低温条件保存。扩增结束后,采用8 μL的电泳样量、核酸染色、2%的琼脂糖凝胶成电泳,随后在紫外透射仪下检测扩增出的产物结果,照相保存并做记录。
表1 用于优化SSR反应体系的影响因子 |
作者贡献
周国雁是本研究的实验设计与数据分析者、论文初稿的撰稿者,李文春参与了本研究的实验设计,是实验研究的具体执行人;伍少云是项目研究的构思者及负责人,指导实验方案的设计、数据分析与论文描写,负责本文的修改。全体作者都阅读并同意最终的文本。
致谢
感谢云南省科技厅“云南省优质高产多抗麦类新品种选育(2010BB005)”项目、云南省农作物资源生物技术创新团队和云南省财政厅—云南省农业科学院专项对本项研究提供了资金资助,也感谢中国农业科学院作物科学研究所李秀全老师为本项研究提供了部分种质资源材料。
参考文献
Beckmann J.S., and Soller M., 1990, Toward a unified approach to genetic mapping of eukarotesbased on sequence tagged nicrosatellite sites, Biotechnology, 8(10): 930-932
http://dx.doi.org/10.1038/nbt1090-930 PMid:1366775
Chai J.F., Liu X., and Jia J.Z., 2006, A rapid isolation method of wheat DNA suitable for PCR analysis, Zhiwu Yichuan Ziyuan Xuebao (Journal of Plant Genetic Resources), 7(2): 246-248 (柴建芳, 刘旭, 贾继增, 2006, 一种适于PCR扩增的小麦基因组DNA快速提取法, 植物遗传资源学报, 7(2): 246-248
Chen Q.F., 1999, Discussion on origin of Chinese endemic wheat, Guizhou Nongye Kexue (Guizhou Agricultural Sciences), 27(1): 20-25 (陈庆富, 1999, 中国特有小麦起源探讨, 贵州农业科学, 27(1): 20-25)
Chen Q.F., Yen C., and Yang J.L., 1998, Chromosome location of the gene for brittle rachis in the Tibetan weedrace of common wheat, Genetic Resources and Crop Evolution, 45: 407-410
http://dx.doi.org/10.1023/A:1008603608879 http://dx.doi.org/10.1023/A:1008635208146
Dieffenbach C.W., and Dveksler G.S., eds., Huang P.T., Yu W.Y., and Chen T.M., trans., 1998, PCR Primer: a laboratory manual, Science Press, Beijing, China, pp.294 (迪芬巴赫C.W., 德维克斯勒G.S., 主编, 黄培堂, 俞炜源, 陈添弥, 主译, 1998, PCR技术实验指南, 科学出版社, 中国, 北京, pp.294)
Dong Y.C., Zhen D.S., Qiao D.Y., Zeng X.Q., En Z.C., and Chen X.R., 1981, Expedition and investigation of Triticum aestivum ssp. yunnanense King, Zuowu Xuebao (Acta Agronomica Sinica), 7(3): 145-151 (董玉琛, 郑殿升, 乔丹杨, 曾学琦, 恩在诚, 陈勋儒, 1981, “云南小麦”(Triticum aestivum ssp. yunnanense King)的考察与研究, 作物学报, 7(3): 145-151)
Katzir N., Danin-Poleg Y., Tzuri G., Karchi Z., Lavi U., and Cregan P.B., 1996, Length polymorphism and homologies of microsatellites in several Cucurbitaceae species, Theor. Appl. Genet., 93(8): 1282-1290
http://dx.doi.org/10.1007/BF00223461
Li M.J., 2004, Current research situation on epidemic system of wheat stripe rust in Yunnan Province, Zhiwu Baohu (Plant Protection), 30(3): 30-33 (李明菊, 2004, 云南省小麦条锈病流行体系的研究现状, 植物保护, 30(3): 30-33)
Li M.J., and Wu S.Y., 2005, Preliminary study of resistance to stripe rust of germplasm resources including local common wheats of high protein and endemic wheat in Yunnan, Mailei Zuowu Xuebao (Journal of Triticeae Crops), 25(3): 23-26 (李明菊, 伍少云, 2005, 云南省高蛋白地方小麦及“铁壳麦”种质资源抗条锈性的初步研究, 麦类作物学报, 25(3): 23-26)
Li M.J., and Wu S.Y., 2006, Assessment to adult-plant resistance to stripe rust of parent materials for quality improvement of wheat germplasms in Yunnan, Mailei Zuowu Xuebao (Journal of Triticeae Crops), 26(1): 113-116) (李明菊, 伍少云, 2006, 云南小麦品质改良亲缘材料成株期抗条锈性评价, 麦类作物学报, 26(1): 113-116)
Lin W.M., eds., 1993, PCR technology operation and application guide, Surgeon Publishing House, Beijing, China, pp.7-14 (林万明, 编著, 1993, PCR技术操作和应用指南, 人民军医出版社, 中国, 北京, pp.7-14)
Sato S., Isobe S., Asamizu E., Ohmido N., Kataoka R., Nakamura Y., Kaneko T., Sakurai N., Okumura K., Klimenko I., Sasamoto S., Wada T., Watanabe A., Kohara M., Fujishiro T., and Tabata S., 2005, Comprehensive structural analysis of the genome of red clover (Trifolium pretense L.), DNA Research, 12: 301-364
http://dx.doi.org/10.1093/dnares/dsi018 PMid:16769692
Shao Q.Q., Li C.S., and Basang C.R., 1980, Semi-wild wheat from Xizang (Tibet), Yichuan Xuebao (Acta Genetica Sinica), 7(2): 149-156 (邵启全, 李长森, 巴桑次仁, 1980, 西藏半野生小麦, 遗传学报, 7(2): 149-156)
Tautz D., 1989, Hypervariability of simple sequence as a general source for polymorphic DNA markers, Nucleic Acids Res., 17(16): 6463-6471
http://dx.doi.org/10.1093/nar/17.16.6463 PMid:2780284 PMCid:318341
Wang H.Y., Wang X.E., Chen P.D., and Liu D.J., 2005, Allelic variation and genetic diversity at HMW glutenin subunits loci in Yunnan, Tibetan and Xinjiang wheat, Zhongguo Nongye Kexue (Scientia Agricultura Sinica), 38(2): 228-233 (王海燕, 王秀娥, 陈佩度, 刘大钧, 2005, 云南、西藏与新疆小麦高分子量谷蛋白亚基组成及遗传多样性分析, 中国农业科学, 38(2): 228-233)
Wang H.Y., Wang X.E., Chen P.D., and Liu D.J., 2007, Assessment of genetic diversity of Yunnan, Tibetan, and Xinjiang wheat using SSR markers, Yichuan Xuebao (Journal of Genetics and Genomics), 34(7): 623-633 (王海燕, 王秀娥, 陈佩度, 刘大钧, 2007, 利用SSR标记分析云南、西藏和新疆小麦的遗传多样性, 遗传学报, 34(7): 623-633)
Wang Z.Q., and Zheng Y.L., 2004, Advances on the study of Tibetanum semi-wild wheat, Mailei Zuowu Xuebao (Journal of Triticeae Crops), 24(4): 133-135 (王志清, 郑有良, 2004, 西藏半野生小麦研究进展, 麦类作物学报, 24(4): 133-135)
Watanabe N., Takesada N., Fujii Y., and Martinek P., 2005, Comparative Mapping of Genes for Brittle Rachis in Triticum and Aegilops, Czech J. Genet. Plant Breed., 41(2): 39-44
Wu S.Y., and Feng Y.B., 2001, Preliminary study on drought resistance of Triticum aestivum ssp yunnanense King, Zhiwu Yichuan Ziyuan Kexue (Journal of Plant Genetic Resources), 2(2): 27-30 (伍少云, 奉有壁, 2001, 云南小麦(Triticum aestivum ssp yunnanense King)的抗旱性鉴定研究初报, 植物遗传资源科学, 2(2): 27-30)
Xia M., Luan F.S, and Li J.P., 1999, Study on influencing factors of RAPD and optimization of RAPD experiment conditions, Zhiwu Yanjiu (Bulletin of Botanical Research), 19(2): 195-200 (夏铭, 栾非时, 李景鹏, 1999, RAPD影响因素的研究及实验条件的优化进展, 植物研究, 19(2): 195-200)
Yang J.H., Yu Y.X., Liu L., Cheng G., Hu Y.X., 2007, HMW-GS compositions and genetic diversities in Triticum aestivum ssp yunnanense King, Zhiwu Yichuan Ziyuan Xuebao (Journal of Plant Genetic Resources), 8(3): 275-279 (杨金华, 于亚雄, 刘丽, 程耿, 胡银星, 2007, 云南铁壳麦高分子量麦谷蛋白亚基组成及其遗传多样性分析, 植物遗传资源学报, 8(3): 275-279)
Yu Y., Chen H.S., and Ge X.J., 2003, Optimization of experiment conditions and primer screening with ISSR markers, Redai Yaredai Zhiwu Xuebao (Journal of Tropical and Subtropical Botany), 11(1): 15-19 (余艳, 陈海山, 葛学军, 2003, 简单重复序列区间(ISSR)引物反应条件优化与筛选, 热带亚热带植物学报, 11(1): 15-19)